Projeto do IPT, em parceria com a IBB e a Embrapii, busca novos alvos genéticos para o desenvolvimento de formulação farmacêutica para terapia gênica da psoríase
O Instituto de Pesquisas Tecnológicas (IPT), por meio dos Laboratórios de Biotecnologia Industrial e de Processos Químicos e Tecnologia de Partículas, iniciou no mês de outubro as atividades do projeto de Pesquisa, Desenvolvimento e Inovação (PD&I) denominado Nanocarreadores para Terapia Gênica, que tem como objetivo principal mapear novos alvos para o desenvolvimento de uma formulação farmacêutica para tratamento da doença psoríase, em parceria com a IBB (Indústria Brasileira de Bionanotecnologia) e a Embrapii.
O projeto emprega uma plataforma tecnológica de mapeamento genético e síntese de nanocarreadores para a encapsulação do material genético de interesse, com mecanismo de ação envolvido no metabolismo da doença. “Nossa pesquisa está direcionada para o desenvolvimento de formulação com ênfase na encapsulação de material genético e com foco na utilização de tecnologias como os sistemas de nanocarreadores, visando a permeação celular para o silenciamento gênico”, completa a gerente técnica do Laboratório de Biotecnologia Industrial e coordenadora do projeto, Patricia Leo.
Terapia gênica é o tratamento de doenças baseado na transferência de material genético. Em sua forma mais simples, a terapia gênica consiste na inserção de genes funcionais em células com genes defeituosos, para substituir ou complementar esses genes causadores de doenças. A maioria das tentativas clínicas de terapia gênica atualmente é para o tratamento de doenças adquiridas, como neoplasias malignas e doenças cardiovasculares, mais do que para doenças hereditárias – no caso da psoríase, uma doença autoimune, ocorre um desequilíbrio imunológico, e a doença se manifesta, na maior parte dos indivíduos, entre os 20 e 40 anos.
Em alguns protocolos, a tecnologia da transferência gênica vem sendo usada para alterar fenotipicamente uma célula de tal modo a torná-la antigênica e, assim, desencadear uma resposta imunológica. De maneira análoga, um gene estranho pode ser inserido em uma célula para servir como um marcador genotípico ou fenotípico, que pode ser usado tanto em protocolos de marcação gênica quanto na própria terapia gênica.

“O panorama atual indica que a terapia gênica não se limita às possibilidades de substituir ou corrigir genes defeituosos, ou eliminar seletivamente células marcadas. Pode-se regular a expressão de genes usando outras moléculas que não o DNA, como, por exemplo, o RNA de interferência ou algum outro tipo de microRNA”, afirma a pesquisadora do IPT – é bom lembrar que no mês de outubro os biólogos norte-americanos Gary Ruvkun e Victor Ambros receberam o Prêmio Nobel em medicina ou fisiologia em razão da descoberta do microRNA e seu papel crucial na forma como os organismos multicelulares crescem e vivem.
As metas pretendidas do projeto são determinar as sequências genéticas que possam provocar o silenciamento da expressão gênica de(s) alvo(s) da doença pesquisada; sintetizar estas sequências; desenvolver os nanocarreadores, para administrar a sequência terapêutica, que serão entregues às células alvos a serem definidas no projeto, e executar os testes in vitro para a liberação da sequência terapêutica nanoencapsulada, com protocolos terapêuticos.
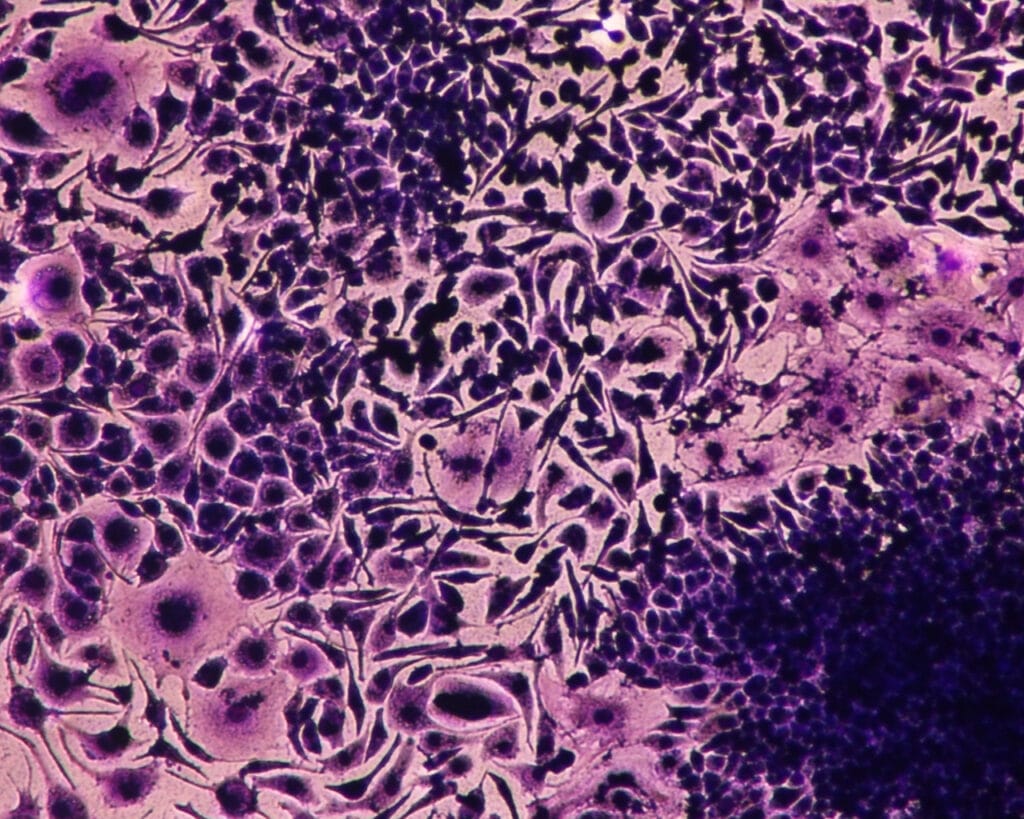
MÉTODOS DE TRANSFERÊNCIA – Segundo a Psoríase Brasil – Associação Brasileira de Psoríase, Artrite Psoriásica e de outras Doenças Crônicas de Pele, a psoríase é uma doença inflamatória, sistêmica e crônica que causa placas avermelhadas espessas na pele, cobertas por escamas esbranquiçadas ou prateadas. Essas lesões podem apresentar coceira, dor, queimação e descamação. Inchaços e rigidez nas articulações podem também ocorrer.
A doença afeta profundamente a qualidade de vida dos pacientes, indo além da questão estética da pele: apesar de não ser contagiosa, a psoríase afeta a autoestima e a qualidade de vida do paciente. Até o momento, não existe uma cura para a psoríase; os tratamentos disponíveis atualmente variam de medicações tópicas (cremes e pomadas) e fototerapia (banhos de luz) a medicações orais e injetáveis.
Segundo a pesquisadora do IPT, a etapa básica envolvida em qualquer aplicação da terapia gênica é a transferência da molécula de DNA ou RNA para a célula alvo. A maneira mais simples de transferir genes para células e tecidos é por meio da inoculação de DNA puro, utilizando técnicas como microinjeção, eletroporação e o método biobalístico.
Métodos mais elaborados e mais eficientes incluem a administração de material genético encapsulado (lipossomos, por exemplo) ou vetores virais, que são as partículas virais empacotando um material genético de interesse. A palavra vetor (que deriva do latim vector, ou seja, aquele que carrega, entrega) define o agente que constitui ou contém os genes a serem transferidos e expressos em uma célula receptora. Os diversos tipos de vetores são utilizados com o objetivo de levar o material terapêutico ao núcleo das células-alvo ou ao citoplasma.
Uma questão-chave da terapia gênica é a escolha do vetor adequado a cada situação. “Um vetor ideal seria aquele que pudesse acomodar um tamanho ilimitado de material genético inserido, fosse disponível em uma forma concentrada, pudesse ser facilmente produzido e ser direcionado para tipos específicos de células, não permitisse replicação autônoma do DNA ou RNA e fosse não tóxico e não imunogênico”, explica a pesquisadora. “Tal vetor ainda não existe e nenhum dos sistemas de entrega de DNA atualmente disponíveis para transferência gênica in vivo é perfeito com respeito a qualquer um desses pontos”.
A vetorização do material genético, que também pode ser descrita como o carreamento do ativo e liberação em áreas específicas do organismo, resulta em maior disponibilidade biológica e redução dos efeitos colaterais, permitindo maior eficácia. Novos ativos de origem biológica, como, por exemplo, aqueles empregados na terapia gênica, requerem novas tecnologias para serem administrados de modo que se tenha a minimização dos efeitos colaterais e a melhoria da aceitação pelo paciente.
“Avanços nessas áreas irão requerer desenvolvimentos paralelos no desenho de vetores, antes que os conhecimentos possam ser utilizados na prática clínica. Da grande quantidade e criatividade dos sistemas de vetores e métodos de transferência gênica que estão sendo desenvolvidos, parece claro que, no futuro, haverá a escolha de métodos diferentes para as diferentes aplicações clínicas. Isso certamente ampliará as oportunidades para o uso da terapia gênica no contexto clínico”, afirmam os pesquisadores do projeto . “Neste contexto da veiculação de material genético, o tópico de vetores é, sem dúvida, o mais crítico para o avanço de alternativas terapêuticas no sentido da aplicação à prática médica”.
ESTUDO EPIDEMIOLÓGICO – Em colaboração com a IBB, os pacientes selecionados para o estudo serão agrupados e selecionados conforme critérios clínicos da doença, tratamento recebido e uma série de parâmetros que serão estabelecidos pela equipe. “Essa etapa é fundamental para garantir a qualidade dos dados das etapas subsequentes: a não definição dos critérios levaria a uma grande variabilidade das amostras coletadas e a um grande viés nos dados analisados”, ressalta a equipe técnica envolvida no projeto.
Para o estudo do perfil genético dos pacientes, a IBB será a responsável pela coleta das amostras dos pacientes selecionados. No IPT, serão realizados ensaios de extração gênica e preparação das amostras para o sequenciamento gênico e caracterização do perfil genético dos pacientes brasileiros perante os bancos de dados de mutações relacionadas à doença já caracterizadas em outros estudos presentes na literatura. Dessa forma será possível entender o cenário genético local da doença.
Com base no escopo apresentado e utilizando-se o padrão de medida de maturidade tecnológica (Technology Readiness Level – TRL) o projeto pretende partir de TRL 3 (estabelecimento de função crítica de forma analítica ou experimental e/ou prova de conceito) e ser entregue à IBB na TRL 6 (demonstração de funções críticas do protótipo em ambiente relevante). O prazo para execução do projeto é de 36 meses, e os recursos financeiros e econômicos necessários totalizam o valor de R$ 8,9 milhões.